No sistema de elementos, o átomo de carbono tem uma posição única e importante, que é a pedra angular da vida. E ele não apenas sustenta todas as formas de vida na Terra, mas também impulsiona a inovação na ciência dos materiais. Aprofundar-se na estrutura do átomo de carbono pode fornecer informações sobre a lógica interna da origem da vida e da inovação material.
Informações básicas sobre o carbono
Número atômico, símbolo químico e massa atômica do carbono
O número atômico do carbono é 6 e o símbolo químico é C. Como o carbono ocorre na natureza na forma de muitos isótopos, sua massa atômica relativa é calculada como uma média baseada na abundância relativa de cada isótopo, que é cerca de 12,01.
Isótopos de carbono
Na natureza, o carbono se apresenta em três isótopos principais: carbono-12, carbono-13 e carbono-14. O carbono-12 é o mais comum, representando cerca de 98,93% de todo o carbono, cujo núcleo contém seis prótons e seis nêutrons. Isso o torna um padrão para a definição de unidades de massa atômica. O carbono-13 compõe cerca de 1,07% do núcleo atômico e tem seis prótons e sete nêutrons. Ele pode ser usado com frequência na espectroscopia de ressonância magnética nuclear (RMN) para ajudar os cientistas a estudar a estrutura molecular. O carbono-14 é um isótopo radioativo com um núcleo composto por seis prótons e oito nêutrons. Ele tem uma meia-vida de cerca de 5.730 anos e desempenha um papel fundamental na arqueologia. Os arqueólogos podem datar artefatos medindo a quantidade de carbono-14 que se decompõe neles.
Análise da estrutura do átomo de carbono
Modelos atômicos e desenvolvimento teórico
Desde o modelo de esfera sólida de Dalton, passando pelo modelo de pudim de ameixa de Thomson, até o modelo nuclear de Rutherford. Assim como o modelo de órbita em camadas de elétrons de Bohr e os modelos modernos de mecânica quântica, a compreensão humana da estrutura atômica foi aprofundada. Esses desenvolvimentos teóricos estabeleceram a base para revelar a estrutura dos átomos de carbono. E os modelos modernos de mecânica quântica sugerem que os elétrons não se movem em órbitas fixas, mas são distribuídos ao redor do núcleo em uma nuvem de probabilidade.
Detalhes da estrutura atômica do carbono
Núcleo atômico
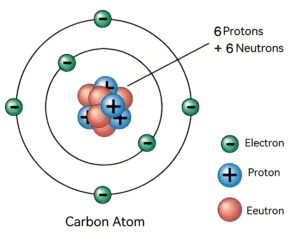
O núcleo de um átomo de carbono é composto de prótons e nêutrons, os prótons têm carga positiva e os nêutrons são eletricamente neutros. Devido à presença de prótons, o núcleo como um todo é carregado positivamente. E como o número de cargas positivas é igual ao número de cargas negativas carregadas pelos elétrons fora do núcleo, o átomo inteiro é eletricamente neutro.
Elétrons estranhos
Os átomos de carbono têm seis elétrons extranucleares, que são distribuídos em diferentes camadas de elétrons de acordo com seus níveis de energia. A primeira camada (camada K) contém até dois elétrons. A segunda camada (camada L) contém até oito elétrons, e a disposição eletrônica dos átomos de carbono é 2,4. Ou seja, a camada K tem dois elétrons e a camada L tem quatro elétrons. Esses quatro elétrons de valência dão ao átomo de carbono suas propriedades químicas exclusivas, permitindo que ele forme compostos estáveis com outros átomos.
Diversas estruturas de carbono
Alótropos de carbono
Diamante
É um cristal duro, com átomos de carbono por meio de ligações covalentes para construir uma estrutura tetraédrica tridimensional, cada átomo de carbono conecta quatro átomos adjacentes. Isso confere ao diamante dureza e ponto de fusão ultra-altos, tornando-o o material preferido para corte, esmerilhamento e outros setores. Além disso, seu brilho intenso também o torna uma gema preciosa.
Grafite
Ele tem uma estrutura em camadas e os átomos de carbono na camada formam uma rede hexagonal de ligações covalentes. A combinação de forças fracas de van der Waals entre as camadas faz com que o grafite tenha boa condutividade elétrica e lubricidade. E você pode usar com frequência grafite na fabricação de eletrodos, lubrificantes e pontas de lápis.
Fulerenos e nanotubos de carbono
Fullerenos são moléculas em forma de gaiola compostas de átomos de carbono, e a mais famosa é o C60, que tem o formato de uma bola de futebol. Os nanotubos de carbono consistem em átomos de carbono em uma estrutura tubular com excelentes propriedades mecânicas, elétricas e de condutividade térmica. Eles podem ser usados para fabricar materiais compostos de alto desempenho e dispositivos eletrônicos.
Estruturas moleculares de carbono
Estrutura molecular do dióxido de carbono
A molécula de CO2 consiste em 1 átomo de carbono e 2 átomos de oxigênio, os átomos de carbono e os átomos de oxigênio são conectados por ligações duplas, em linha reta. Essa estrutura torna o dióxido de carbono gasoso em temperatura e pressão ambiente. Ele é uma parte importante do ciclo de carbono da Terra e o principal gás de efeito estufa responsável pelo aquecimento global.
Compostos orgânicos
Os compostos orgânicos são compostos que contêm carbono, mas não incluem o monóxido de carbono, o dióxido de carbono e os carbonatos. As propriedades quadruvalentes dos átomos de carbono permitem que ele forme uma variedade de compostos orgânicos com hidrogênio, oxigênio, nitrogênio e outros átomos. Eles formam a base dos materiais vitais, como proteínas e ácidos nucleicos.
Conceitos especiais em estruturas de carbono
Átomos de carbono terciário
Os átomos de carbono terciários conectam três átomos de carbono e têm atividade reativa especial na química orgânica. Na reação de substituição nucleofílica de hidrocarbonetos halogenados, os hidrocarbonetos halogenados que contêm átomos de carbono terciários seguem principalmente o mecanismo SN1. Essa propriedade é diferente dos hidrocarbonetos halogenados primários e secundários, que são amplamente usados na síntese orgânica.
Estrutura atômica das fibras de carbono
Fibra de carbono é composto de microcristais de grafite, os átomos são dispostos ao longo do eixo axial da fibra. Por isso, ela tem vantagens de alta resistência e baixa densidade. Com essas propriedades, pode ser amplamente utilizada na indústria aeroespacial, na fabricação de equipamentos esportivos e em outros campos.
Descoberta e aplicações do carbono
Quem descobriu o carbono
O carbono é um dos primeiros elementos descobertos e utilizados pelos seres humanos. Já na pré-história, os seres humanos usavam carvão vegetal como combustível. Entretanto, foi somente no século 18 que o químico francês Lavoisier provou experimentalmente que o carbono era um elemento. E, com base no latim "carbo", ele lhe deu o nome de "carbono", que significa carvão.
Dez usos do carbono
Combustível
Quando queimados, os combustíveis à base de carbono, como madeira e carvão, reagem com o oxigênio. Em seguida, ele pode liberar calor para aquecimento, cozimento e geração de energia.
Produção de aço
A quantidade adequada de carbono pode aumentar a resistência e a dureza do aço. Ao regular o teor de carbono, é possível produzir diferentes propriedades do aço e usá-lo na construção e na fabricação de máquinas.
Eletrodo de grafite
Eletrodo de grafite tem boa condutividade elétrica e resistência a altas temperaturas. Pode ser usado nos elos condutores de fornos elétricos de fabricação de aço, alumínio eletrolítico e outros setores.
Chumbo de lápis
A grafite do lápis é feita de grafite misturado com argila, e a estrutura da camada de grafite permite que ele deixe marcas no papel ao escrever.
Adsorção de carvão ativado
O carvão ativado tem poros ricos, grande área de superfície específica, que pode absorver impurezas e substâncias nocivas. E você pode usá-lo na purificação de água e ar e em outros cenários.
Joias com diamantes
O diamante é um alótropo do carbono, que tem brilho intenso, alta dureza e é frequentemente usado em joias.
Material de fibra de carbono
Tem alta resistência e baixa densidade, sendo usado na fabricação de equipamentos aeroespaciais e esportivos para reduzir o peso e melhorar o desempenho.
Aprimoramento da borracha
A adição de negro de fumo à borracha pode aumentar sua força, resistência ao desgaste e resistência ao envelhecimento, que é usada principalmente na fabricação de pneus.
Conservação de alimentos
O carvão ativado pode absorver odores e gases nocivos em embalagens de alimentos e aumentar a vida útil dos alimentos.
Produtos eletrônicos
Também é possível usar amplamente o carbono em produtos eletrônicos, como o grafeno. Ele tem excelentes propriedades elétricas e espera-se que seja usado em futuros dispositivos eletrônicos.
Conclusão
O átomo de carbono tem uma estrutura única, natureza rica e ampla aplicação. Ele foi encontrado desde os materiais básicos da vida até os materiais científicos e tecnológicos de ponta. O estudo aprofundado da estrutura dos átomos de carbono promoveu o desenvolvimento da sociedade humana e ajudou a criar um futuro melhor.