Hoewel ze allebei koolstof zijn, kunnen grafiet en grafeen niet meer van elkaar verschillen. Ze hebben een aantal speciale eigenschappen waardoor ze waarschijnlijk op verschillende gebieden worden gebruikt. In dit artikel leer je meer over hun structuren, toepassingen en kosten. Laten we er eens in duiken.
Inhoudsopgave
Schakel
Grafiet vs Grafeen
Wat is grafiet
Grafiet (een koolstofallotroop) Blad van koolstof is een zeshoekig raster. Het gladde gevoel dat grafeen geeft, komt doordat de lagen over elkaar heen glijden. Grafiet is nu te vinden in alledaagse voorwerpen, van onze potloden tot smeermiddelen en zelfs batterijen. Het is nog steeds een geleider (maar niet zo geleidend als grafeen, omdat het gelaagd is). Omdat het goedkoop is en relatief veel voorkomt, is het een uitstekende kandidaat voor veel industriële toepassingen.
Wat is grafeen
Grafeen is een honingraatstructuur van koolstofatomen in een enkele laag. Het is ook maar één atoom dik, wat betekent dat het materiaal superdun kan zijn en toch heel sterk. Het wordt vaak het "wondermateriaal" genoemd vanwege zijn lichtheid en bijna-transparantie, maar ook omdat het sterker is dan alles wat we ooit zijn tegengekomen met een respectabel elektrisch geleidingsvermogen. Het is 200 keer sterker dan staal en slechts één atoom dik. De toepassingen zijn talrijk, van elektronica tot medische apparatuur, en hoewel het materiaal relatief veel voorkomt in de natuur is het maken ervan kostbaar en moeilijk geweest.
Structuur
Lagen vs Enkele laag
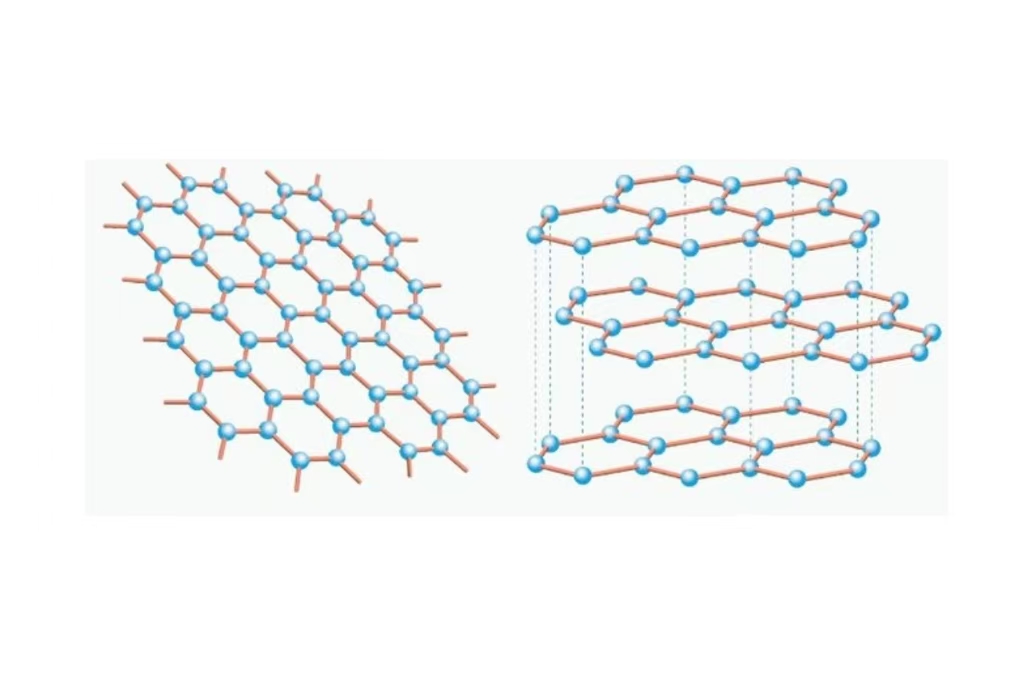
Grafiet: Bestaat uit talrijke lagen koolstofvellen die over elkaar gestapeld zijn. Omdat deze lagen zwak met elkaar binden, kunnen ze gemakkelijk over elkaar glijden. Daarom voelen we grafiet in onze hand als glad en gedraagt het zich ook als een smeermiddel.
Grafeen: Een enkele honingraatlaag van koolstofatomen, een één atoom dik materiaal met uitzonderlijke sterkte en flexibiliteit.
Verschillen in hechting
Grafiet: Omdat de lagen bij elkaar worden gehouden door primitieve van der Waals krachten, is grafiet gemakkelijk te splitsen of te splijten.
Grafeen: Deze koolstofatomen zijn zeer nauw met elkaar verbonden binnen de enkele laag, wat grafeen zijn formidabele sterkte en flexibiliteit geeft.
Eigenschappen van grafiet en grafeen
Elektrische geleidbaarheid
Grafiet: Terwijl grafiet ook elektriciteit overdraagt dankzij vrij bewegende elektronen tussen zijn lagen, zijn die zonder extra grafeenvellen hier niet zo geleidend. De weerstand ontstaat wanneer de lagen voldoende ver uit elkaar liggen.
Grafeen: Een van de bekendste elektrische geleiders Omdat elektronen er vrijwel zonder weerstand doorheen kunnen stromen, is grafeen een natuurproduct voor hogesnelheidselektronica.
Mechanische sterkte
Grafiet: Zacht en bros. Grafiet breekt gemakkelijk, daarom wordt het gebruikt voor potloodstiften. Wordt gemakkelijk bros omdat de lagen slechts door zwakke bindingen bij elkaar worden gehouden.
Grafeen: Het is extreem sterk, 20 keer zo robuust als staal. Hoewel het slechts één koolstofatoom dik is, is de structuur van grafeen te danken aan het sterke kristallijne rooster en omdat elke C-C binding een sterkte heeft die gelijk is aan die van tweemaal de lengte.
4.3Thermische geleidbaarheid
Grafiet: Fatsoenlijk warmtegeleidingsvermogen, wordt daarom op grote schaal gebruikt voor bijvoorbeeld passieve koeling.
Grafeen: Uitstekende thermische geleidbaarheid. Het is een van de beste geleiders van thermische energie, dus een goede keuze voor het koelen van elektrische componenten.
Toepassingen
Grafiet
Potloden: Potloden gebruiken grafiet als "lood" omdat het niet te veel vlekt en gemakkelijk op een oppervlak markeert en vervolgens uitwist wanneer dat nodig is. Grafiet bestaat uit vellen in een laag, dus ze kunnen met heel weinig druk schrijven en een markering op papier achterlaten.
Smeermiddelen: Omdat het glad is, wordt het gebruikt in smeermiddelen om wrijving tussen machines te voorkomen. Omdat de lagen grafiet glad zijn, glijden ze gemakkelijk over elkaar heen en vormen ze een stevige barrière waardoor onderdelen minder snel slijten door beweging.
Batterijen: Grafiet blijkt ook een intrinsiek element te zijn dat twee primaire functies kan vervullen in de anode van een lithium-ion batterij: stabiliteit en efficiënte energieopslag. Door deze gelaagde structuur kunnen lithiumionen gemakkelijk in- en uitstromen tijdens laad-/ontlaadcycli.
Staalproductie: Tijdens de staalproductie wordt het over het algemeen toegepast als vuurvast materiaal omdat het bestand is tegen grote hitte. Om dit te doen, isoleert voeringen in gieterijen en coatingovens moet een constante temperatuur behouden - een absolute vereiste voor de productie van staal van hoge kwaliteit.
Grafeen
Elektronica: Omdat grafeen een uitstekende geleider van elektriciteit is, kan het volgens twee nieuwe experimenten van Berkeley Lab en UC San Diego gebruikt worden in plaats van silicium in computerchips - waardoor snellere apparaten mogelijk worden die koeler werken en (idealiter) minder energie per berekening verbruiken. De hoge elektronenmobiliteit maakt het bij uitstek geschikt voor de snelle schakelsnelheid die nodig is in toekomstige computertechnologieën.
Medische apparaten: Biocompatibiliteit en gevoelige grafeigenschappen maken het ideaal voor biosensoren, systemen voor het toedienen van medicijnen en weefselengineering, enz. De niet-giftigheid en compatibiliteit met biologische systemen maken het aantrekkelijk voor gebruik in medische diagnostiek of therapeutische behandelingen.
Energieopslag: Supercondensatoren en geavanceerde batterijen kunnen in de toekomst grafeen gebruiken om sneller op te laden en meer energie op te slaan. Door het grote oppervlak en de hoge geleidbaarheid kunnen de prestaties van energieopslagapparaten worden verbeterd, waardoor ze langer meegaan.
Composietmaterialen: Grafeen kan worden gecombineerd met andere materialen zoals metalen en kunststoffen om ze lichter en tegelijkertijd sterker of elektrisch geleidend te maken. Potentiële toepassingen van deze met grafeen versterkte composieten zijn gewichtsvermindering, verhoging van de brandstofefficiëntie en verbetering van de algehele ablatieprestaties.
Grafiet vs. grafeen: kosten
Grafiet: Laag
Overvloed: Grafiet is goedkoop beschikbaar in gewone, natuurlijke vorm, wereldwijd gedolven, het is een gemakkelijk beschikbaar en kostenefficiënt mineraal.
Productiekosten: Door de lage productie- en verwerkingskosten is grafiet ook geschikt voor gebruik in veel industriële toepassingen.
Grafeen: Hoog
Productie-uitdagingen: Het produceren van grafeen is aanzienlijk moeilijker dan het produceren van grafiet. Hoewel h-BN met een monolaag nu kan worden bereid met natte methoden, blijven de bestaande fabricagemethoden - zoals chemische dampdepositie (CVD) en exfoliatietechnieken - duur en niet gemakkelijk schaalbaar voor productie op grote schaal. Het blijft duur en is niet gemakkelijk schaalbaar voor productie op grote schaal.
Prijstrends: Ondanks de dalende trend in de grafeenprijzen zijn de kosten van dit materiaal veel hoger dan die van grafiet. Er wordt momenteel gewerkt aan kosteneffectievere manieren om grafeen te produceren, zodat het materiaal commercieel levensvatbaar wordt.
Conclusie
Grafiet en grafeen hebben een aantal unieke eigenschappen die op elkaar lijken, waardoor het een belangrijke groep materialen is. Daarom kunnen we grafeen beschouwen als de laatste stap in de evolutie van koolstof. Grafiet heeft decennialang industrieën gediend, maar grafeen is volgens velen de echte gamechanger die veel gebieden in verschillende sectoren kan ontwrichten. Als mensen grafeen goedkoper en eenvoudiger kunnen produceren dankzij het huidige onderzoek, is een wereld waarin het buitenaardse materiaal koning is misschien niet zo ver weg. Of je nu respect hebt voor het pragmatisme van grafiet of je nu laat verleiden door het potentieel van grafeen. Beide zullen moeten samenwerken om verder te komen in de technologie en industrie.