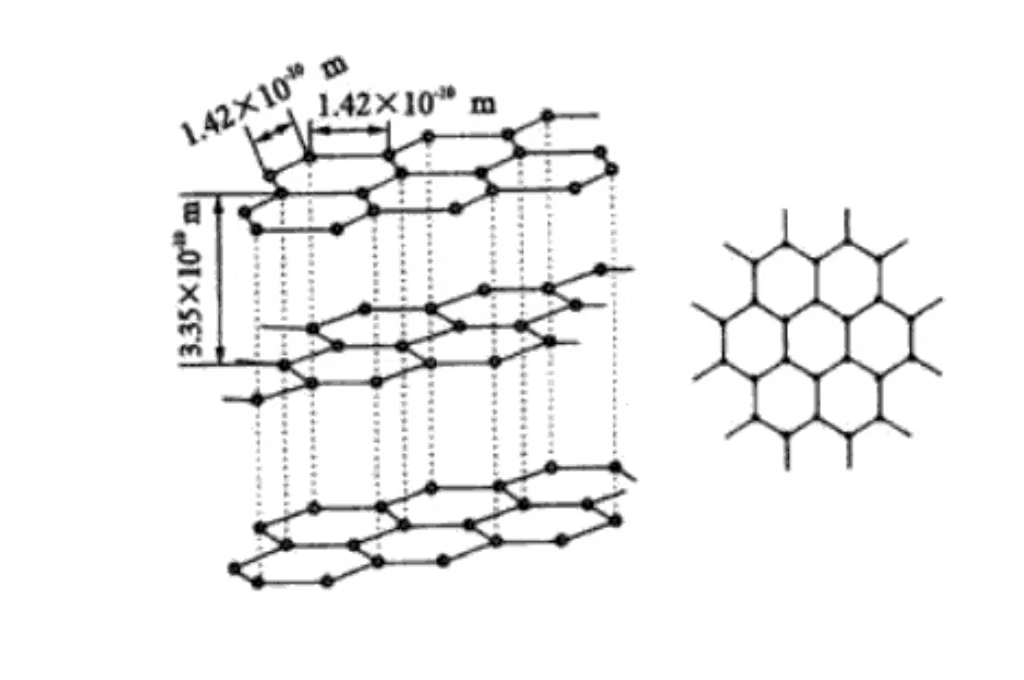
石墨作为碳的一种重要同素异形体,在许多领域都发挥着重要作用。对石墨结构的深入探索是开启石墨广泛应用潜力和开发新材料的关键。
目录
切换
什么是石墨?
石墨是一种由碳原子组成的矿物,在自然界分布广泛。它具有金属光泽和柔软光滑的手感。因此,它是制作铅笔芯的理想材料。石墨的颜色多为黑色或深灰色。其纯度和结晶度因形成环境而异。
石墨的原子和分子结构
石墨的原子结构
石墨的主要成分是碳。石墨中的碳原子通过共价键连接。而每个碳原子与周围的三个碳原子形成稳定的六角环结构,并在平面上无限延伸,形成坚实的原子骨架。
石墨的分子结构
在分子水平上,石墨由以下成分组成 层数 由碳原子堆叠而成。层间碳原子由相对较弱的范德华力维持。这种层状结构解释了为什么石墨具有极佳的润滑性和层间易滑动性。
石墨结构的两个关键要素
石墨六方晶体结构
安排
石墨具有六方晶体结构,碳原子在平面上呈六边形紧密排列,其中的夹角为 120 度。这种排列规则而稳定,有利于电子传导,是其良好导电性的基础。
分层
碳原子以平行平面堆叠,层间距约为 0.335nm。层与层之间的范德华力很弱,这使得石墨易于在外部层之间滑动,具有润滑性。在机械制造领域,石墨常用作润滑剂。
晶体结构层
每一层碳原子通过共价键形成一个网络平面。这些碳原子在空间有序排列,形成了石墨的宏观晶体特征和各向异性。石墨层中的强共价键使石墨在平面上具有较高的强度和硬度。由于层间作用力较弱,垂直面方向的强度较低。
碳原子内的键
范德瓦耳力量
层间碳原子依靠的范德华力很弱,因此石墨层间容易滑动分离,具有润滑性。但这也使得石墨的层间结构在某些条件下(如高温高压)会发生变化。例如,它可以转变为金刚石结构。
分层
由于范德华力很弱,施加微小的剪切力就能使石墨层分离。这不仅体现了润滑性,还为插层反应创造了可能,通过插层反应可以改变石墨的物理和化学性质,从而制备出特殊的复合材料。如锂离子电池的负极材料。
共价键
层中的碳原子通过共价键紧密相连,形成稳定的六边形结构。这就决定了石墨在平面内具有较高的硬度和强度,保证了其在电极材料应用中的结构稳定性。同时,它还限制了电子的运动,影响了平面内的各向异性。
Sp2 杂交
债券角度
碳原子采用 sp2 杂化,一个 2s 和两个 2p 轨道杂化形成三个等效的 sp2 杂化轨道。这些轨道分布在一个角度约为 120 度的平面三角形中。这样,碳原子与相邻的三个碳原子形成稳定的共价键,构建成六边形结构,有利于电子的脱ocalization传导和良好的导电性。
碳原子
碳原子通过 sp2 混合轨道与周围的三个碳原子构建了一个平面骨架。π电子云使石墨具有良好的导电性,其中的电子可随电场变化而自由移动。并使石墨在化学反应中变得活跃,参与电化学过程。如作为锂离子电池中的电子传递介质。
各向异性
平面内属性和平面外属性
石墨在不同方向上表现出明显的各向异性。在平面内,共价键很强,具有高硬度、高强度和良好的导电性。如可以用石墨纤维增强复合材料作为增强相,利用其平面内的抗拉强度。在垂直面方向,由于层间范德华力弱,强度低,导电性差。这一特性使其在不同的应用场景中发挥了针对性的优势。
原子能安排
石墨碳原子按照特定规律排列,在平面上形成六边形,在空间上形成堆积层。这种排列方式决定了石墨的晶体结构以及物理和化学性质。X 射线衍射可以根据其有序排列所呈现的特定模式来确定其结晶度和结构参数。原子排列的稳定性使石墨在一定的温度和压力范围内保持稳定的性能。如石墨作为耐火材料在高温下可保证结构的完整性,为工业应用的可靠性提供保障。
石墨的晶格和晶体结构
石墨的晶格结构
石墨具有六方晶格结构,a 轴和 b 轴等长。且夹角为 120 度,c 轴垂直于碳原子平面。其长度反映了层状结构的周期性排列,属于六方晶系,具有特定的对称性和晶体学特征。
石墨晶体结构
石墨晶体由许多六边形晶格单元组成,在空间中有序排列。内部碳原子以高度有序的方式排列。缺陷和杂质会显著改变石墨的性能,影响电子和声子传输、化学反应和材料的均匀性。
石墨结构中的三种常见缺陷
石墨结构中的缺陷对其性能有很大影响。
空位和间隙原子等点缺陷会破坏原子的完整性,影响电子传导和机械性能。
线性缺陷(如位错)会影响塑性变形和强度。
晶界等表面缺陷会阻碍电子和声子的传输,降低导电性和导热性。而且容易导致化学反应和杂质聚集。
石墨结构相关概念
石墨路易斯结构
石墨的路易斯结构显示了碳原子之间的电子共享,并通过与相邻碳原子形成共价键来满足八电子稳定结构。未参与的电子形成分散的π电子云。这为理解化学键和电子分布提供了基础。
石墨杂化
石墨碳原子的 sp2 杂化是其独特结构和特性的根源。这使得石墨具有平面结构和非局域化的π电子云,从而赋予石墨各种优异的特性。
石墨符号和公式
石墨的化学符号是 "C"。虽然用简单的分子式难以表达大分子结构,但在化学计算和反应式中。C "可以代表石墨的反应,反映碳的转化和守恒。
石墨结构和结合
石墨的层状结构和表面特性对其键合特性具有重要意义。层间范德华力很弱,因此有必要对石墨表面进行改性或选择合适的粘合剂来增强其相互作用。表面改性可以引入官能团或进行粗化处理。粘合剂的极性基团可以与石墨表面的碳原子紧密结合。在复合材料中,良好的结合性能是保证整体机械性能和功能特性的关键。而粘结不良则容易造成界面应力集中,导致材料失效。
解释石墨和其他材料的结构差异
石墨结构与石墨烯结构的对比
事实上 石墨烯 代表一原子厚的石墨层。在每 1 毫米厚的石墨片中,大约有 300 万层石墨烯叠加在一起。石墨烯可以被看作是一层石墨,而石墨是由多层石墨烯叠加而成的。
石墨和钻石结构的比较
结构差异
金刚石的碳原子采用 sp3 杂化,形成四面体空间结构,原子间的共价键非常牢固。石墨为 sp2 杂化平面六面体,呈层状,层与层之间的范德华力很弱。
性能差异
结构上的差异导致了性能上的明显不同。金刚石硬度很高,用于机械加工;石墨质地柔软,润滑性好,用作润滑剂和铅笔芯。石墨导电,金刚石不导电。金刚石折射率高,透明度高,用于珠宝首饰;石墨呈黑色,不透明。
石墨结构类型
天然石墨
它通常出现在石墨片岩、石墨片麻岩、含石墨片岩和变质页岩中。根据晶体形态 天然石墨 石墨可同时分为两种:晶质石墨(又分为鳞片石墨和隐晶质石墨,也称为土质石墨)。
合成石墨
合成石墨 是一种化学产品。其主要成分是碳。它是通过对有机聚合物进行高温热解和石墨化而得到的。
特殊石墨结构,如可膨胀石墨和纳米石墨结构。可膨胀石墨经特殊处理,层间插入材料,在高温下分解膨胀,具有良好的阻燃性,用于防火材料。纳米石墨结构,如纳米石墨片和纳米石墨纤维,比表面积大,表面活性高,机械性能优良。它在储能、催化剂载体和高性能复合材料领域具有巨大潜力。
石墨结构与用途之间的相关性
石墨的独特结构决定了它的广泛用途。良好的导电性使其成为一种电极材料,可用于电池和电解池。高温稳定性和化学惰性使其成为钢铁工业的耐火材料。润滑性使其在机械制造中充当润滑剂。在航空航天领域,石墨复合材料因其低密度、高强度和热稳定性而被用于制造飞机和火箭部件。此外,石墨还在铅笔制造、石墨烯制备等领域发挥着重要作用。而每一种应用都与石墨结构密切相关。
结论
石墨的结构从多个维度展现了其独特性和复杂性,深刻影响着石墨的性能和应用。对石墨结构的深入研究和理解,为石墨在材料科学和能源等诸多领域的创新应用开辟了广阔的前景。这将有助于解决现代社会的材料和能源问题。